Rezumat
Diabetul zaharat de tip 2 reprezintă una din cauzele principale de boală cronică de rinichi. Opţiunile terapeutice pentru tratamentul diabetului la pacienţii cu boală cronică de rinichi sunt limitate din cauza reducerii ratei de filtrare glomerulară şi consecutiv a riscurilor date de asocierea agenţilor antidiabetici.
Această lucrare prezintă aspecte ale managementului terapeutic al unei paciente cu diabet zaharat de tip 2 şi boală cronică de rinichi la care antidiabeticele orale nu mai reprezentau o opţiune şi care după iniţierea insulino-terapiei şi a schimbării stilului de viaţa şi-a îmbunătăţit în mod semnificativ parametrii metabolici.
Cuvinte cheie: diabet zaharat, boală cronică de rinichi, terapie antidiabetică
MEDICAL PRACTICE
CLINICAL LESSONS
Therapeutic options in patients with diabetes and advance stage chronic kidney disease
Abstract
Type 2 diabetes mellitus represents a leading cause of chronic kidney disease worldwide. The therapeutic options for diabetes treatment in patients with chronic kidney disease are limited due to the reduced glomerular filtration rate and subsequently the associated risks of antidiabetic agents.
This paper presents the therapeutic management of a Type 2 diabetes mellitus in a female patient who was diagnosed with chronic kidney disease. Oral antidiabetic agents were no longer an option for her and, after initiating insulin therapy and lifestyle modification, metabolic parameters significantly improved.
Keywords: diabetes mellitus, chronic kidney disease, antidiabetic therapy
Introducere
La nivel mondial, diabetul zaharat de tip 2 (DZ tip 2) reprezintă una dintre cauzele principale care conduc la apariția bolii cronice de rinichi (BCR) (1,2). Ţintele de terapie pot fi dificil de atins datorită opțiunilor terapeutice limitate date de scăderea ratei de filtrare glomerulare. Cel mai important efect secundar este hipoglicemia. Pe de altă parte, controlul glicemic favorabil la pacienții cu DZ tip2 este esențial pentru reducerea riscului de complicații (microvasculare și macrovasculare) și pentru reducerea progresiei BCR (3,4). Există restricții importante în legatură cu utilizarea tiazolidindionei, metforminului, sulfonilureelor, agoniștilor de GLP-1 și a inhibitorilor de SGLT2 în contextul asocierii la DZ a BCR (5-7).
Descrierea cazului
Pacientă în vârstă de 62 de ani, pensionară (profesoară), din mediul rural, cu ereditate diabetică (tatăl a avut DZ tip 2), cu un făt macrosom (4100g), cunoscută cu diabet zaharat tip 2 în evoluţie din 2008 actual în tratament cu antidiabetice orale, s-a prezentat în clinica de diabet a Institutului “NC Paulescu”, București.
Motivele internării au fost: valori glicemice crescute, hipoglicemii uşoare în jurul orei 10 dimineața în zilele când îşi administrează gliclazidul dar omite micul dejun şi parestezii în “şoseta” la nivelul membrelor inferioare bilateral predominant nocturne.
Pacienta este necompliantă la dietă şi are un stil de viaţa sedentar. Asociază hipertensiune arterială gradul III (2007), boală cardiac ischemică – angină de efort (2013), pielonefrită cronică, infecţii urinare recurente, dislipidemie cu hipercolesterolemie (2008), obezitate grad I, colecistectomie (2013).
Ultima schemă de tratament recomandată a fost metformin 100mg, 2cp/zi, gliclazid 60 mg 2cp/zi, atorvastatina 10 mg, 1 cp/zi şi indapamid 1,5 mg, 1cp/zi.
Tabelul1. Valorile parametrilor ce definesc echilibrul metabolic, funcția renală și tratamentul din istoricul pacientei
| Anul | |||||||
| Parametru | 2008 | 2013 | 2015 | 2016 | |||
| Glicemie à jeun | 147 | 153 | 175 | 170 | |||
| Glicemie postprandială | *d.l. | 198 | *d.l. | *d.l. | |||
| G (kg) | 89 | 84 | 89 | 93 | |||
| IMC (kg/m2) | 31.52 | 29.76 | 31.53 | 32.95 | |||
| HbA1c (%) | 7 | 7,7 | 6.9 | 8,3 | |||
| RFG (ml/min) | 60 | 60 | *d.l. | dl | |||
| Colesterol total | 224 | 198 | *d.l. | 258 | |||
| Terapie recomandată | |||||||
| Metformin | 2g/zi | ||||||
| Gliclazid | 60mg/zi | 120 mg/zi | |||||
*d.l.=date lipsă
Examenul clinic relevă o înălţime de 168 de cm, greutate 93 kg, BMI 32.95 kg/m2, circumferinţa abdominală de 102 cm, TA=130/75 mmHg, AV=86 bpm, parestezii în”şosetă’’ şi sensibilitate termică şi dureroasă diminuată la nivelul membrelor inferioare bilateral, fără alte modificări.
Examenele biologice de laborator au decelat o glicemie a jeun de 236 mg/dl, o HbA1c de 9,7%, Colesterol total=245 mg/dl, LDLc=157.6mg/dl, trigliceride=287mg/dl, HDLc=39 mg/dl (trat. cu atorvastatină 10mg/zi), creatinina serică=1.5 mg/dl, eRFG (MDRD)=35 ml/min/1.73m2, raport albumina/creatinină urinară=51 mg/g crea/zi, urocultura sterilă.
S-a efectuat examenul fundului de ochi care a confirmat prezenţa retinopatiei diabetice neproliferative medii ambii ochi.
Indicele gleznă-braț a avut valoarea 1 bilateral.
Coroborând analizele de laborator cu cele paraclinice am constatat la această pacientă prezenţa complicaţiilor microvasculare: retinopatia diabetică neproliferativă medie, polineuropatia diabetică senzitivă simetrică distală şi boală cronică de rinichi G3bA2 KDIGO (RFG= 42ml/min/1.73m2) (de etiologie mixtă: diabetică şi pe fond de pielonefrită cronică).
Discuții
Cazul prezentat ne pune în față o pacientă cu diabet zaharat tip 2 tratat cu antidiabetice orale ce prezintă variabilitate glicemică, cu un control glicemic slab (HbA1c 9.2%) ce asociază obezitate şi dislipidemie aterogenă, cu complicaţii microvasculare (polineuropatie şi retinopatie diabetică) şi macrovasculare (boală cardiacă ischemică) deja constituite la care se decelează o eRFG de 35 ml/min/1.73m2.
În cazul acestei paciente intervenţia terapeutică optimă trebuie să asigure o reducere susţinută a HbA1c cu aproximativ 2% (<7.5%), cu evitarea hipoglicemiilor severe, care să ne ofere siguranţa cardiacă şi renală cu efect neutru/benefic pe profilul lipidic, pe tensiunea arterială şi pe greutate, cu limitarea progresiei complicaţiilor şi bineînţeles care să asigure o aderenţă crescută la tratament din partea pacientei (Tabelul 2).
Opțiunile terapeutice sunt relativ limitate pentru această pacientă. Datorită prezenței bolii cronice de rinichi (GFR = 35 ml / min / 1,73mp), metforminul nu mai este indicat și având în vedere riscul crescut de hipoglicemie și creștere în greutate, administrarea de sulfoniluree a fost întreruptă. De asemenea, este recomandat ca inhibitorii SGLT2 să fie restricționați la pacienții cu insuficiență renală moderată până la severă (pacienți cu EGFR <60 ml / min / 1,73 m2) (9). În acest caz, prezența obezității ar putea reprezenta o indicație pentru exenatida cu eliberare prelungită, dar la pacienții cu insuficiență renală moderată (clearance-ulcreatininei 30-50 ml / min) administrarea nu este recomandată datorită dovezilor clinice insuficiente.
Având în vedere toate aceste aspecte, s-a decis inițierea terapiei cu insulină bazală cu titrarea dozei până la atingerea unui profil glicemic favorabil și menținerea metforminului cu reducerea dozei la 1 g pe zi. La început, pacienta a refuzat terapia cu insulină, dar împărțirea aceluiași compartiment cu alți pacienți a reprezentat un factor benefic pentru acceptarea ulterioară a tratamentului.
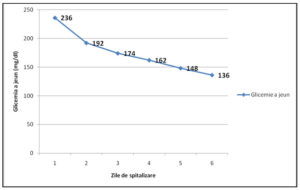
Rolul medicului a fost, de asemenea, important, în sensul că el a oferit timp și resurse de instruire unui pacient inițial necompliant (7, 8, 10). Astfel, după inițierea terapiei cu insulină, pacientul a prezentat o scădere a valorilor glicemice a jeun (Figura 1).
Figura 1. Evoluţia valorilor glicemiei à jeun pe parcursul internării după inițierea insulinoterapiei
Obiectivele terapeutice sunt rezumate în Tabelul 2. Conform acestor obiective, pacienta a fost consiliată și au fost recomandate schimbarea stilului de viață cu efectuarea exercițiu fizic de minimum 150 min/săptămână, distribuite în cel puțin trei zile/săptămână, cu pauze de cel mult două zile între exerciții (mersul pe jos, bicicleta și înotul).
Tablelul 2.Obiective terapeutice
| Parametrii | Intervale terapeutice |
| Glicemia à jeun | 90-130mg/dl |
| Glicemia postprandială | <180mg/dl |
| HbA1c | <7.5% |
| LDLc | <100mg/dl |
| HDLc | >40mg/dl |
| Trigliceride | <150mg/dl |
| Tensiune arterială | <135/85mmHg |
| Greutate | Scădere iniţială de 10% din G actuală |
Din punct de vedere al intervenției medical nutriţionale, am recomandat o dietă de 1700kcal/zi, care conține 230 g HC/zi, dintre care proteinele de 60 g/zi (0,8 g/kg corp, 15% din totalul total energetic) lipide 56 g/zi (30% din cerința energetică globală), optând pentru o reducere a aportului de proteine din cauza bolii renale. În ceea ce privește compoziția dietei cu acizi grași, am indicat: acizi grași saturați (FA) <10% din totalul energetic, FA monosaturați = 10-12%, polinesaturați FA = 6-10%, trans FA <1% de 30-45 g/zi.
În ceea ce privește aportul de sare, scăderea consumului de clorură de sodiu la mai puţin de 3 g/zi are un efect benefic în primul rând asupra patologiei cardiovasculare a pacientului. Hidratareaeste, de asemenea, esențială, 1500-2000 ml / zi, de preferință apă, ajută la menținerea stării fiziologice renale.
Pacienta a primit recomandări referitoare la controlul diabetului zaharat: cum se auto-monitorizează glicemia, cu indicarea determinării zilnice a glicemiei a jeun și a metodei de ajustare a dozelor de insulină și să monitorizeze hemoglobina glicozilată (HbA1c) la fiecare trei luni.
Pentru comorbiditățile asociate, a fost recomandat un tratament cu inhibitor al enzimei de conversie (prestarium 10 mg 1cp/zi), diuretic (indapamid 1,5 mg 1cp/zi), doză de statină a fost crescută (atorvastatină 40 mg, 1cp/zi), acizi grași omega-3 1 g, 2 cp/zi, neurotrofic (acid alfa-lipoic 600 mg, 1 cp/zi) și acid acetilsalicilic 75 mg 1 cp/zi.
După externare, pacienta a revenit la reevaluare după cinci luni, cu o evoluție bună. Senzația de anxietate simțită la începutul terapiei cu insulină a evoluat într-o stare de optimism, pacientul recunoscând importanța respectării regimului de tratament. A schimbat stilul de viață, urmând regimul indicat în proporție de până la 70%, iar stilul de viață sedentar a fost înlocuit cu plimbări zilnice de câte 30 de minute, împreună cu seturi de exerciții aerobice de 20-30 de minute la fiecare trei zile, acasă. În tabelul 3 sunt prezentate parametrii biologici la momentul internării și la reevaluarea de la 5 luni.
Tabelul 3. Evoluția parametrilor clinici și biologici la 5 luni
| Parametru | Mai 2017 | Septembrie 2017 |
| G (kg) | 93 | 90 |
| IMC (kg/m2) | 32.95 | 31.88 |
| Glicemii à jeun (mg/dl) | 150-200 | 90-150 |
| Glicemii postprandiale (mg/dl) | 200-300 | 100 – 180 |
| HbA1c (%) | 9,2% | 7,4 % |
| Episoade de hipoglicemie | prezenţe | absente |
| Colesterol plasmatic (mg/dl) | 245 | 163 |
| Trigliceride plasmatice (mg/dl) | 287 | 184 |
| LDL (mg/dl) | 157.6 | 81.2 |
| HDL (mg/dl) | 39 | 45 |
| Creatinină serică (mg/dl) | 1.3 | 1.22 |
| RFG (ml/min/1.73m2) | 42 | 45 |
| TA (mmHg) | 130/75 | 125/70 |
| Parestezii | prezente | ameliorate |
Concluzii
În cazul pacienților cu diabet zaharat tip 2 complicat cu boală cronică renală avansată, opțiunile terapeutice sunt relativ limitate, iar tratamentul unor astfel de cazuri reprezintă o adevărată provocare pentru medici (7, 11-13). Astfel, există o nevoie urgentă de studii care ar putea demonstra siguranța noilor antidiabetice orale și injectabile în cazul bolii renale avansate.
O altă problemă apare din inerția clinică a inițierii terapiei cu insulină. Această se datorează adesea atât pacientului, cât și medicului. În acest context, evaluarea psihologică și consilierea sunt aspecte semnificative care ar trebui să facă parte din managementul integrat al pacientului cu diabet zaharat. Doctorul alege de multe ori să întârzie inițierea terapiei cu insulină tocmai pentru că pacientul nu este compliant, este anxios şi, pe de altă parte, în ambulatoriu, timpul pentru consultații nu este suficient pentru educația terapeutică necesară. În plus, psihologul, care ar trebui să facă parte din echipă interdisciplinară extinsă, de multe ori nu există.
Asistenta medicală şi dieteticianul pot ajuta pacientul cu câteva ore de educaţie cu privire la monitorizarea corectă a glicemiei, adoptarea unui stil de viaţa sănătos şi implementarea intervenţiei nutriţionale (9, 10). Din păcate, atât educatorul cât şi dieteticianul nu se regăsesc în ambulatoriu, cel mai adesea, nici măcar în clinicile medicale specializate și, prin urmare, aceste aspecte ale educaţiei devin, de asemenea, responsabilitatea medicului, care, va acordă prea puțină atenție altor elemente esențiale care ar putea schimba radical evoluția bolii (10, 12, 13).
Conflict de interese: nu există
Acknowledgments: Toţi autorii au avut contribuţie egală la acest articol
Bibliografie
- Hill NR, Fatoba ST, Oke JL, Hirst JA, O’Callaghan CA, Lasserson DS, Richard Hobbs FD. Global Prevalence of Chronic Kidney Disease – A Systematic Review and Meta-Analysis. Remuzzi G, ed. PLoS ONE 2016; 11(7):e0158765.
- Tuttle KR, Bakris GL, Bilous RW, Chiang JL, de Boer IH, Goldstein-Fuchs J et al. Diabetic Kidney Disease: A Report from an ADA Consensus Conference. Diabetes Care 2014; 37(10): 2864-2883.
- Willis K, Cheung M, Slifer S. KDIGO 2012 Clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney International Supplement 2013; 3(1):1-150.
- Kramer H, Molitch ME. Screening for kidney disease in adults with diabetes. Diabetes Care. 2005; 28: 813–1816.
- Voiculescu D, Andrei CL, Busnatu SS, Badiu DC, Sinescu CJ. Thyrotoxicosis and electrical storms of a diabetic heart.In INTERDIAB 2016: DIABETES MELLITUS AS CARDIOVASCULAR DISEASE Book Series: International Conference on Interdisciplinary Management of Diabetes Mellitus and its Complications. 2016.p 512-520.
- Flynn C, Bakris G. Noninsulin glucose‐lowering agents for the treatment of patients on dialysis. Nat Rev Nephrol 2013; 9: 147–153.
- Cavanaugh KL. Diabetes management issues for patients with chronic kidney disease. Clin Diabetes 2007; 25: 90–97.
- Lostun, A, Lostun, G, Hainarosie R. A Retrospective Study of Non-violent Deaths and Diagnostic Discrepancies Over a Period of Three Years. Revista de chimie 2016; 67(8); 1587-1590.
- Inzucchi SE, Bergenstal RM, Buse JB, Diamant M, Ferrannini E, Nauck M et al. Management of hyperglycemia in type 2 diabetes: a patient-centred approach. Position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2012; 35: 1364–1379.
- Kelley L, Wick A. Pharmacotherapy of Type 2 Diabetes Mellitus: Navigating Current and New Therapies. Medsurg Nursing 2015; 24(6): 413.
- Philip A, McFarlane. Maturing Clinical Experience with SGLT2 Inhibitors Is Clarifying Clinical Applications. Available from: http://www.mednet.ca/en/report/maturing-clinical-experience-with-sglt2-inhibito.html [Accessed 25th March 2018].
- Badiu CD, Rahnea Nita G, Ciuhu AN, Manea C, Smarandache CG, Georgescu DG et al. Neuroendocrine renal carcinoma therapeutic and diagnostic issues. Acta Endocrinologica-Bucharest 2016; 12(3); 355-361.
- Lostun A, Keresztesi A, Hainarosie R, Lostun Gl. Medical Negligence – Is There a Defined Pattern? Revista de Chimie 2016; 67(12):2425-428.
MEDICAL PRACTICE
CLINICAL LESSONS
Therapeutic options in patients with diabetes and advance stage chronic kidney disease
Introduction
Casus description
The patient, a women aged 62, retired, a former teacher, from the rural area, with hereditary diabetes (the father had T2DM), with a macrosomic fetus (4100g), was diagnosed with T2DM ten years before the current admission, until when she was following oral antidiabetics treatment. After signing the informed consent form, she was admitted to the Diabetes Clinic of the National Institute of Diabetes, Nutrition and Metabolic Diseases “NCPaulescu” in Bucharest, Romania, claiming increased glycemic values, mild hypoglycemia in the morning (in the context of gliclazide administration and breakfast omission) and typical lower limbs bilateral paresthesia, with nocturnal predominance. It is worth mentioning that the patient was not compliant with the nutritional recommendations; she led a sedentary lifestyle and deliberately refused to initiate insulin therapy, a fact which complicated the underlying pathology. From her personal pathological history, she mentioned: third-degree arterial hypertension (2007), ischemic cardiac disease – effort angina (2013), chronic pyelonephritis, recurrent urinary infections, dyslipidemia with hypercholesterolemia (2008), first-degree obesity, cholecystectomy (2013).
The last recommended treatment regimen was metformin 100 mg 2cps/day, gliclazide 60 mg 2cps/day, atorvastatin 10 mg 1 cp/day and indapamid 1.5 mg 1cp/day.
In Table 1 discrete values of some parameters related to metabolic balance, kidney function and treatment from the patient history are shown.
On clinical examination, the patient weighted 93 kg, BMI was 32.95 kg/m2, abdominal circumference 102 cm, blood pressure 130/75 mmHg, heart rhythm 86 bpm, “sock” paresthesia, low thermal and painful sensitivity at the level of both lower limbs, without further modifications. Biological laboratory examinations revealed a fasting glycemia of 236 mg/dl, a HbA1c of 9.7%, mixed dyslipidemia (total cholesterol 245 mg/dl, LDLc 157.6mg/dl, triglycerides 287mg/dl, HDLc 39 mg/dl) in treatment with atorvastatin 10mg/day, nitrogen retention syndrome (serum creatinine 1.5 mg/dl, GFR (MDRD) = 35 ml/min/1.73m2), albumin/ urinary creatinine ratio = 51 mg/g creatinine/day, sterile urine culture. The eye fundus examination revealed the presence of medium non-proliferative diabetic retinopathy in both eyes. The determination of the ankle-arm index recorded a value of 1, bilaterally.
Corroborating the laboratory test results with the clinical ones the presence of microvascular complications was detected: medium non-proliferative diabetic retinopathy, symmetrical distal sensory diabetic polyneuropathy and chronic renal disease G3bA2 KDIGO (GFR= 42ml/min/1.73m2) of mixed etiology: diabetes with underlying chronic pyelonephritis
Table 1. Discrete values of parameters related to metabolic balance, kidney function and treatment from patient’s history
| Year | |||||||
| Parameter | 2008 | 2013 | 2015 | 2016 | |||
| Fasting glycemia | 147 | 153 | 175 | 170 | |||
| Postprandial glycemia | *M.d. | 198 | *M.d. | *M.d. | |||
| W (kg) | 89 | 84 | 89 | 93 | |||
| BMI (kg/m2) | 31.52 | 29.76 | 31.53 | 32.95 | |||
| HbA1c (%) | 7 | 7,7 | 6.9 | 8,3 | |||
| GFR (ml/min/1.73mp) | 60 | 60 | *d.l. | dl | |||
| Total cholesterol | 224 | 198 | *d.l. | 258 | |||
| Treatment | |||||||
| Metformin | 2g/day | ||||||
| Gliclazid | 60mg/day | 120 mg/day | |||||
*d.l.=date lipsă*M.d.= missing data
Discussions
The proposed case presents a female patient with T2DM, who associated CKD (eGFR=35ml/min/1.73m2), obesity, atherogenic dyslipidemia, microvascular (diabetic polyneuropathy and retinopathy) and macrovascular complications (coronary artery disease). She was treated with oral antidiabetics, with whom she did not attain glycemic control (HbA1c 9.2%).
For this patient, the optimum recommendations include a therapeutic intervention which could ensure a sustained reduction of HbA1c by approximately 2% (7-7.5%), with avoidance of severe hypoglycemias. This would be globally beneficial and would grant cardiac and renal safety with neutral/beneficial effect on the lipid profile, blood pressure and weight, limiting the evolution of complications, absent/reduced adverse effects (avoiding severe hypoglycemias) and, of course, which should ensure an increased adherence to treatment (Table 2).
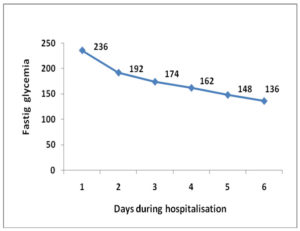
The therapeutic options are relatively limited for this patient. Due to the CKD (GFR=35ml/min/1,73mp) metformin was no longer indicated and given the increased risk of hypoglycemia and weight gain, sulphonylurea administration was interrupted. Also, it is recommended that SGLT2 inhibitors should be restricted in patients with moderate to severe renal failure (patients with eGFR< 60 ml/min/1.73 m2) (9). In this case, the presence of obesity could represent an indication for prolonged-release exenatide, but in patients with moderate renal failure (creatinine clearance 30 – 50 ml/min) administration is not recommended due to insufficient clinical evidence. Given all these aspects, it was decided to initiate baseline insulin therapy with dose titration until the achievement of a favorable glycemic profile and to maintain metformin intake with dose reduction to 1g/day. In the beginning, the patient refused the insulin therapy, but sharing the same ward with other patients represented a beneficial factor for the subsequent acceptance of the treatment. The role of the doctor was also important, in the sense that he provided time and training resources to an initially non-compliant patient (7, 8,10). Thus, after the initiation of insulin therapy, the patient experienced a decline in fasting glycemic levels (Fig. 1)
Figure 1. Fasting glycemic trend during hospitalization after initiating insulin therapy
The therapeutic objectives are summarized in Table 2. According to these goals the following recommendations were given. A change of sedentary lifestyle with physical exercise of minimum 150 min/week, distributed in at least three days/week, with breaks not longer than two days in between the exercises (walking, bicycle riding, and swimming).
From the point of view of the medical-nutritional intervention, we recommended a diet of 1700kcal/day, comprising 230g HC/day, out of which proteins 60g/day (0.8g/body kg, 15% of the overall energetic total), lipids 56g/day (30% of the overall energetic requirement), opting for a reduction of protein intake because of the kidney disease. In terms of diet composition of fatty acids, we recommended: saturated fatty acids (FA) < 10% of the energetic total, monounsaturated FA = 10-12%, polyunsaturated FA = 6-10%, trans FA < 1% and fiber intake of 30-45 g/day. Regarding salt intake, lowering the consumption of NaCl to less than 3 g/day has beneficial effect first of all on the cardiovascular pathology of the patient. Hydration is also essential, the use of 1500-2000 ml/day, preferably water, helps maintain the renal physiological status.
The patient was given instruction related to diabetes control: how to self-monitor glycemia, with the indication of the daily determination of fasting glycemia and postprandial glycemia, how to adjust insulin dosages and to monitor glycosylated haemoglobin (HbA1c) every three months.
Table 2. Therapeutic objectives for various parameters related to metabolic control
| Parameter | Therapeutic interval |
| Fasting glycemia | 90-130mg/dl |
| Postprandial glycemia | <180mg/dl |
| HbA1c | <7.5% |
| LDLc | <100mg/dl |
| HDLc | >40mg/dl |
| Triglycerides | <150mg/dl |
| Blood pressure | <135/85mmHg |
| Weight | Initial decrease with 10% |
For the associated comorbidities, a treatment with conversion enzyme inhibitor was recommended (Prestarium 10 mg 1cp/day), diuretic (Indapamide 1.5mg 1cp/day), the statin dose was increased (Atorvastatin 40mg, 1cp/day), omega-3 polyunsaturated fatty acids 1g, 2 cp/day, neurotrophic (alpha-lipoic acid 600 mg, 1 cp/day) and acetylsalicylic acid 75 mg 1cp/day.
After discharge, the patient returned for the check-up after five months with good evolution. The anxiety feeling felt initially at the onset of the insulin therapy has evolved into a state of optimism, the patient acknowledging the importance of being compliant with the treatment regime. She also changed her lifestyle, following the indicated regimen up to 70%, and the sedentary lifestyle was replaced with daily walks of 30 minutes each, 2-3 times/day along with aerobic exercise sets of 20-30 minutes every three days, done at home (Table 3).
Table 3. The evolution of metabolic parameters within five months from the discharge
| Parameter | May 2017 | September 2017 |
| W (kg) | 93 | 90 |
| BMI (kg/m2) | 32.95 | 31.88 |
| Fasting glycemic levels (mg/dl) | 150-200 | 90-150 |
| Postprandial glycemic levels (mg/dl) | 200-300 | 100 – 180 |
| HbA1c (%) | 9,2 % | 7,4 % |
| Episodes of hypoglycemia | present | absent |
| Total cholesterol level (mg/dl) | 245 | 163 |
| Plasma triglyceride level (mg/dl) | 287 | 184 |
| LDL (mg/dl) | 157.6 | 81.2 |
| HDL (mg/dl) | 39 | 45 |
| Serum creatinine (mg/dl) | 1.3 | 1.22 |
| RFG (ml/min/1.73m2) | 42 | 45 |
| BP (mmHg) | 130/75 | 125/70 |
| Paresthesia | present | improved |
Conclusions
In case of patients with diabetes mellitus with complications of the advanced chronic renal disease, the therapeutic options are relatively limited, and the management of such cases is a real challenge for doctors (7, 11-13). Thus, there is an urging need for studies that could demonstrate the safety of new oral and injectable antidiabetics in case of the advanced renal disease. Another problem arises from the clinical inertia of insulin therapy initiation. It is often due to both the patient and the doctor. In this context, psychologic evaluation and counselling are significant aspects that should be part of the integrated management of the patient with diabetes mellitus.
The doctor often chooses to delay the onset of insulin therapy precisely because the patient is not compliant, is anxious and, on the other hand, on an outpatient basis, the time for consultations is not enough for therapeutic education. Moreover, the psychologist, who should be part of the extended interdisciplinary team, often does not exist. Nurse and dietician may help the patient with some hours of education on the accurate blood glucose monitoring, adoption of a healthy lifestyle and implementation of the nutritional intervention (9-10). Unfortunately, both are not found in the outpatient clinic, most often, not even in specialized medical clinics, and therefore, these aspects of education become also the responsibility of the doctor, who will, therefore, pay too little attention to other essential elements which could radically change the evolution of the disease (10, 13-14).
References are the same as in Romanian version of this article.
Conflicts of interest: none
Received: 3 April 2018
Accepted: 21 May 2018
Acknowledgements: All authors have equal contributions.